[Презентация] ### Введение Галогены представляют собой группу химически активных неметаллов, расположенных в VII группе периодической системы элементов. Они обладают семью электронами на внешнем уровне, что обуславливает их высокую реакционную способность. Электроотрицательность и окислительная активность галогенов уменьшаются от фтора к йоду. ### Физические свойства Состояние галогенов варьируется от газа (фтор и хлор) до жидкости (бром) и твердого вещества (йод и астат). Их цвета также различаются: фтор имеет бледно-желтый цвет, хлор - зеленый, бром - красно-бурый, а йод - фиолетовый. Все галогены хорошо растворяются в воде и органических растворителях. ### Химические свойства Электроотрицательность галогенов высока и уменьшается от фтора к йоду. Они активно участвуют в окислительно-восстановительных реакциях, взаимодействуя с металлами и неметаллами, образуя галогениды. Галогены также способны реагировать с водородом, образуя галогеноводороды. Некоторые галогены, такие как хлор, бром и йод, могут подвергаться диспропорционированию в водных растворах. ### Индивидуальные характеристики Фтор обладает самой высокой реакционной способностью среди галогенов. Он применяется в производстве фторопластов и используется в ядерной энергетике. Хлор широко используется для обеззараживания воды и производства поливинилхлорида (ПВХ). Бром важен для производства антипиренов и фотоматериалов. Йод играет ключевую роль в синтезе гормонов щитовидной железы и используется как антисептик. Астат и теннессин являются редкими радиоактивными элементами, которые изучаются в ядерной медицине. ### Основные соединения Галогеноводороды, такие как HF, HCl, HBr и HI, имеют широкое промышленное применение. Кислородсодержащие кислоты, например, HClO, HClO₂ и HClO₃, также используются в различных отра
Не подходит Презетация?
Создайте свою быстро и легко. Используйте нейросети, готовые шаблоны и голосового ИИ-помощника
Транскрипция презентации
Слайд 1:
Слайд 2: Галогены
Слайд 3: Общая характеристика галогенов
Слайд 4: Расположение в периодической таблице
Слайд 5: Электронная конфигурация
Заберите Презентацию бесплатно FREE
Зарегистрируйтесь и отредактируйте её под свои задачи за пару минут.
Шаблоны презентаций, доступные бесплатно в редакторе Slider Ai
Бесплатные шаблоны в редакторе Slider






Презентация диз...
Текст
Медиа
Фигуры
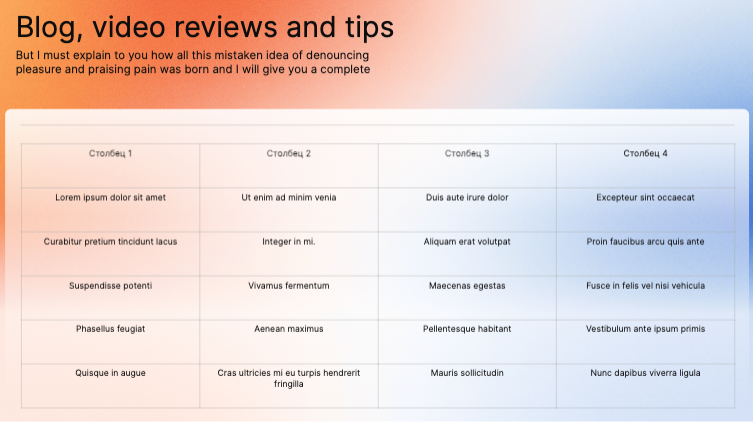
Таблица
Диаграммы
3D модели
500
Создать

Добро
пожаловать
в Slider Ai
пожаловать
в Slider Ai
Нам доверяют

Кирилл В
трафик-менеджер
В редакторе я в основном оформляю свои кейсы для демонстрации клиентам. Как правило, использую готовый шаблон, прикрепляю документы и генерю презентацию как черновик, а потом уже добавляю данные по кейсам в виде диаграмм для наглядности, дорабатываю текст, визуал, но даже так времени это занимает на...

Сергей Н
Руководитель компании
Я в дизайне вообще ничего не понимаю, поэтому мне очень помогает функция, когда я могу просто накидать сырой текст на слайды, а затем все это причесать с помощью ии. Минут за 15 можно сделать аккуратную и стильную презентацию. Это реально сильно экономит силы и время.

Анна К
бренд-менеджер
Slider Ai для нас спасение при подготовке презентаций стратегии и отчетов для клиентов. В отличии от других редакторов, которыми мы с командой пользовались раньше, здесь не нужно быть дизайнером, чтобы создавать красивые презентации, за которые не стыдно перед важными клиентами.

Ирина М
отдел маркетинга
Как руководитель отдела, ценю, что с помощью Slider Ai все презентации команды выходят в едином корпоративном стиле. Это укрепляет бренд и выглядит профессионально. Встроенные диаграммы, особенно каскадные и Ганта, незаменимы для визуализации данных. Настройка бренд-кита заняла у нас 15 минут, и теп...

Ольга М
бизнес-тренер
В редакторе Slider Ai мне проще делать презентации для своих выступлений, потому что нужно по минимуму что-то делать вручную, много функций, которые позволяют просто нажать на кнопку и получить готовый результат. Плюсом есть возможность добавить видео прямо на слайды, а еще использовать 3D модели, р...
Ваша следующая великая работа всего в одном шаге от вас